Per rispettare la scadenza del 29 dicembre 2023, le aziende cosmetiche si preparano a rispettare i nuovi requisiti del Modernization of Cosmetics Regulation Act (MoCRA).
La FDA continua a condividere le linee guida sul nuovo portale di presentazione elettronica, Cosmetics Direct e sul formato di etichettatura strutturata dei prodotti (SPL).
Portale diretto cosmetici
A settembre 2023, la FDA ha pubblicato un nuovo documento di 81 pagine, Electronic Submission Portal Screenshots for Cosmetics . Questo documento fornisce il percorso dell’utente per la registrazione della struttura e l’elenco dei prodotti cosmetici come richiesto da MoCRA.
Mostra anche errori di convalida che possono verificarsi quando si inviano le informazioni.
La FDA ha fatto un ottimo lavoro educando il settore su cosa aspettarsi da MoCRA. Questa anteprima aiuta le aziende a determinare se sono in grado di gestire gli invii del portale o se avranno bisogno di competenze esterne.
La FDA ha iniziato ad accettare commenti sul portale di presentazione elettronica della bozza di recente sviluppo (Cosmetics Direct) e sui moduli cartacei. La scadenza per inviare un commento era il 18 ottobre 2023.
Un formato SPL (Speek Into Structured Product Labeling)
Il nuovo portale Cosmetics Direct evidenzia il formato SPL, un componente chiave del software strutturato di etichettatura dei prodotti, che sarà necessario per tutte le presentazioni cosmetiche. Per le aziende cosmetiche in cui il formato SPL è un nuovo territorio, gli esempi, la formattazione XML e la convalida possono sembrare complicati.
Prima del rilascio delle schermate, le uniche informazioni disponibili per il settore erano nella bozza di guida per il settore. Questa guida ha indicato che è necessario inviare i dati di registrazione ed elenco in formato SPL e ha fornito questi dettagli:
“La registrazione e l’elenco dei prodotti presso la struttura di produzione cosmetica saranno disponibili utilizzando lo stesso processo di presentazione elettronica disponibile per registrare una struttura ed elencare un farmaco presso la FDA. Ciò contribuirà a semplificare il processo di invio delle informazioni di registrazione ed elenco per le strutture cosmetiche e i prodotti per le entità che inviano anche informazioni sulla costituzione di farmaci ed elenco”.
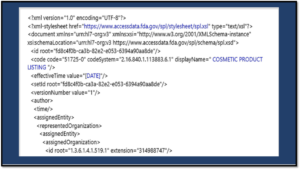
Guida all’implementazione e procedure di convalida SPL
A ottobre, la FDA ha pubblicato una linea guida per l’implementazione e la convalida di SPL. La guida di 275 pagine descrive Cos metics Direct come uno strumento di creazione SPL intuitivo che eseguirà convalide iniziali, creerà e salverà le presentazioni SPL e le invierà alla FDA.
Il 14 novembre, la FDA ha aggiornato la Guida all’implementazione della SPL per includere ulteriori aggiornamenti alle registrazioni delle strutture di prodotti cosmetici e agli elenchi dei prodotti inclusi nel quadro della SPL.
Prossime scadenze di conformità MoCRA
La FDA non ha ancora annunciato la data esatta di lancio del portale di presentazione di Cosmetics Direct. Tuttavia, sarà lanciato in tempo affinché le strutture rispettino la prossima scadenza del 29 dicembre 2023.
La FDA ha annunciato una data di applicazione ritardata del 1° luglio 2024 o sei mesi dopo la scadenza del 29 dicembre. Questo aggiornamento riconosce le complessità delle presentazioni SPL e offre alle strutture cosmetiche più tempo per rispettare i requisiti.
L’estensione si applica alle strutture cosmetiche che hanno iniziato a produrre o a lavorare prodotti cosmetici dopo il 29 dicembre 2022. Invece di doversi registrare entro la scadenza di dicembre, dovranno semplicemente completare la registrazione prima del 1° luglio.
Le aziende che hanno iniziato a commercializzare prodotti cosmetici dopo il 29 dicembre 2022 avranno anche altri sei mesi prima che la FDA applichi i requisiti di quotazione MoCRA.
Il Registrar Corp può aiutare
Grazie alla vasta esperienza di Registrar Corp nell’invio di elenchi di farmaci FDA nel formato SPL, le aziende cosmetiche si affidano a Registrar Corp per garantire la conformità ai nuovi requisiti cosmetici della FDA ai sensi del MoCRA e per assisterle nelle presentazioni di Cosmetics Direct.
Visualizza l’intero documento in anteprima al nuovo portale cosmetici e scopri cosa può fare Registrar Corp per la tua azienda per rispettare le nuove normative.


